Przedstawicielami węglowodorów cyklicznych są m.in. cykloalkany, cykloalkeny i cykloalkadieny. Cykloalkany to węglowodory o budowie pierścieniowej (cyklicznej). Poniżej podano uproszczone wzory wybranych cykloalkanów i ich homologów:
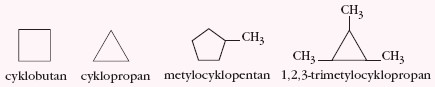
Wśród cykloalkanów najtrwalszy jest cykloheksan, o czym decyduje brak napięcia kątowego w jego cząsteczce. Cyklopropan, cyklobutan, cyklopentan ze względu na występujące napięcie kątowe – zmniejszające się w szeregu zapisanych związków – cechuje mała trwałość pierścienia. Cząsteczki te, zwłaszcza cyklopropan, są bogate w energię i łatwo następuje otwarcie ich pierścienia węglowego.
Analizując wzory sumaryczne tych związków można zauważyć, że tworzą one szereg homologiczny o wzorze CnH2n. Wzór ten jest identyczny ze wzorem szeregu homologicznego alkenów. Cykloalkany i alkeny o identycznej liczbie atomów węgla w cząsteczce są izomerami (izomeria typu łańcuchowo-pierścieniowego).
Przemysłowe otrzymywanie cyklopropanu przedstawiono poniższym równaniem:
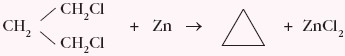
Cykloalkany posiadają wyższe temperatury wrzenia i topnienia niż odpowiadające im łańcuchowe alkany.
Cykloalkany również tworzą izomery. Cykloheksan może tworzyć 2 konformacje – łódkową i krzesełkową, a np. 1,2-dimetylocyklopropan tworzy 2 izomery geometryczne cis i trans.
Cykloalkany uczestniczą w reakcjach substytucji rodnikowej, np.
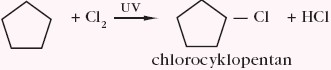
Cykloalkeny są zbudowane z pierścieni zawierających jedno wiązanie podwójne węgiel-węgiel a cykloalkadieny są węglowodorami pierścieniowymi zawierającymi dwa podwójne wiązania węgiel-węgiel, np.
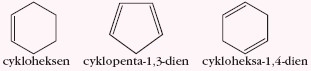
Cykloheksen można otrzymać w reakcji eliminacji wody z cykloheksanolu w odpowiednich warunkach:
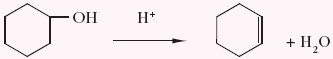
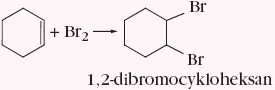
Cykloalkeny i cykloalkadieny jako związki nienasycone biorą udział w reakcjach addycji, np.