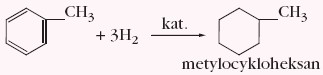Toluen to bezbarwna ciecz o charakterystycznym zapachu. Spala się kopcącym płomieniem.
Toluen można otrzymać w reakcji Würtza-Fittiga:
C6H5 – Cl + CH3 – Cl + 2 Na → C6H5 – CH3 + 2 NaCl
Toluen bierze udział w reakcjach substytucji. Należy jednak pamiętać, że obecna w pierścieniu grupa metylowa –CH3 kieruje nowy podstawnik w określone miejsce w pierścieniu. Ten fakt określany jako tzw. wpływ kierujący podstawników jest powszechny w reakcjach związków aromatycznych.
Toluen jako węglowodór alifatyczno-aromatyczny reaguje z bromem podczas naświetlania. W tych warunkach podstawiony zostaje atom wodoru w grupie –CH3 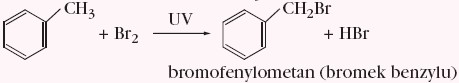
Toluen w obecności silnego utleniacza, np. KMnO4, tworzy kwas benzoesowy, co przedstawiono poniżej ogólnym schematem: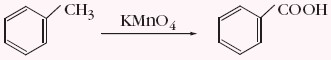
Toluen w określonych warunkach (katalizator) ulega uwodornieniu: