Srebro nie reaguje z tlenem atmosferycznym. Czarny nalot pokrywający z czasem przedmioty srebrne to siarczek srebra(I) – związek ten tworzą obecne w powietrzu śladowe ilości siarkowodoru w reakcji z tlenem i srebrem.
![]()
W szeregu napięciowym metali srebro leży za wodorem. Jako metal o dodatniej wartości potencjału elektrochemicznego srebro nie reaguje z wodą, kwasami słabo utleniającymi oraz z zasadami, reaguje natomiast z kwasami silnie utleniającymi, np.:
![]()
Tlenek srebra(I) to czarny osad. Jest nietrwały – łatwo ulega rozkładowi.
![]()
Tlenek ten wydziela się z roztworu azotanu(V) srebra(I) pod wpływem mocnej zasady:
![]()
gdyż podczas strącania następuje rozkład nietrwałego wodorotlenku.
![]()
Tlenek srebra(I) rozpuszcza się w amoniaku, tworząc wodorotlenek diaminasrebra(I).
![]()
W wyniku działania kwasu solnego na roztwór AgNO3 wytrąca się biały, serowaty osad chlorku srebra(I) ciemniejący na świetle.
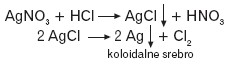
Dodanie do osadu AgCl amoniaku spowoduje rozpuszczenie osadu, a wprowadzenie w następnej kolejności do roztworu kilku kropel kwasu azotowego(V) – wytrącenie białego osadu AgCl.
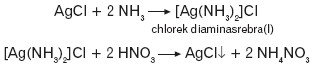
Związki srebra(I) mają właściwości utleniające, co wykorzystano w próbie Tollensa, służącej do wykrywania aldehydów i badania właściwości redukujących cukrów.
