Pełna interpretacja zapisu reakcji chemicznej została opisana w poniższej tabeli:
| N2 + | 3 H2 = | 2 NH3 |
| 1 mol cząsteczek N2 | 3 mole cząsteczek H2 | 2 mole cząsteczek NH3 |
| 6,02 · 1023 cząsteczek N2 | 3 · 6,02 · 1023 cząsteczek H2 | 2 · 6,02 · 1023 cząsteczek NH3 |
| 2 · 14 g = 28 g | 3 · 2 · 1 g = 6 g | 2 · (14 g+ 3 · 1 g) = 34 g |
| 34 g (masa substratów) | 34 g (masa produktu) | |
| stosunek molowy substratów 1:3 | ||
| 22,4 dm3 N2 | 3 · 22,4 dm3 H2 | 2 · 22,4 dm3 NH3 |
| stosunek objętościowy substratów 1:3 | ||
Wydajność reakcji chemicznej:
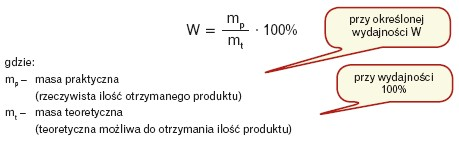
Jeżeli proces chemiczny realizowany jest poprzez kilka etapów o różnej wydajności W1, W2, itd., to wydajność całkowitą procesu należy obliczyć ze wzoru:
W = (W1 /100%) · (W2/100%) · … · 100%
