H2O LH = 2 + ½ (6 – 2 · 1) = 2 + 2 = 4
LH = 4 =>
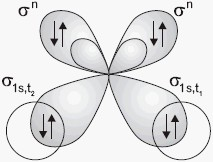
- orbitale walencyjne atomu tlenu są w stanie hybrydyzacji sp3
- ponieważ na atomie tlenu są dwie wolne pary elektronowe, należy uwzględnić fakt, że pary te najsilniej się odpychają, oraz że odpychanie wolna para – para wiążąca jest silniejsze niż para wiążąca – para wiążąca; kąty między wiązaniami σzmniejszają się (104,5°)
- kształt cząsteczki wody nie będzie zgodny z przestrzennym rozmieszczeniem hybryd, z których dwie opisują wolne pary elektronowe => należy uwzględnić odpychanie między odpowiednimi elektronami
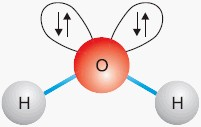
- cząsteczka ma kształt kątowy
 |
 |
