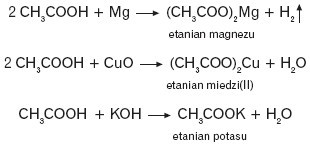
Kwasy karboksylowe, podobnie jak kwasy nieorganiczne, reagują z metalami, tlenkami metali i wodorotlenkami tworząc sole. Reakcje te przebiegają z udziałem atomu wodoru grupy karboksylowej (pęka wiązanie tlen-wodór).
Kwasy karboksylowe w odpowiednich warunkach (np. podwyższona temperatura,obecność enzymów) ulegają dekarboksylacji:
a) kwasy monokarboksylowe:
![]()
b) polikwasy, np. kwasy dikarboksylowe – produkt reakcji uzależniony jest od odległości łańcucha węglowodorowego oddzielającego grupy –COOH od siebie:
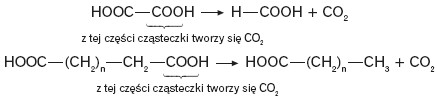
Kwasy karboksylowe w odpowiednich warunkach ulegają redukcji.
![]()
Kwasy karboksylowe wykorzystywane są do otrzymywania bezwodników kwasowych, chlorków i amidów, co przedstawiono ideowo na poniższym schemacie.
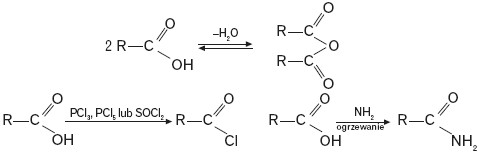
W odpowiednich warunkach (obecność fosforu) kwasy karboksylowe służą do otrzymania chlorowcokwasów, gdyż łatwo reagują z chlorem lub bromem:
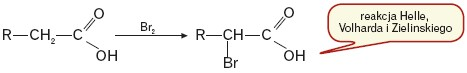
Charakterystyczną właściwością kwasów karboksylowych jest zdolność do reagowania z alkoholami i tworzenia estrów. Reakcja ta przebiega z rozerwaniem wiązania węgiel-tlen grupy karboksylowej (mechanizm reakcji poznano, używając w badaniach izotopu tlenu 18O):
![]()
Przedstawiona ogólnym zapisem reakcja, katalizowana jonami H+, nosi nazwę reakcji estryfikacji. Jest to reakcja odwracalna.
Proces odwrotny do estryfikacji to hydroliza. Hydroliza może zachodzić w obecności mocnego kwasu lub zasady. Należy pamiętać, że hydroliza kwasowa jest prostym odwróceniem reakcji estryfikacji, która również jest katalizowana jonami H+. Hydroliza zasadowa jest procesem nieodwracalnym, gdyż jony OH– są w niej reagentem, a nie katalizatorem.
Poniżej przedstawiono schemat przemian chemicznych, w których jako substrat występuje kwas etanowy.
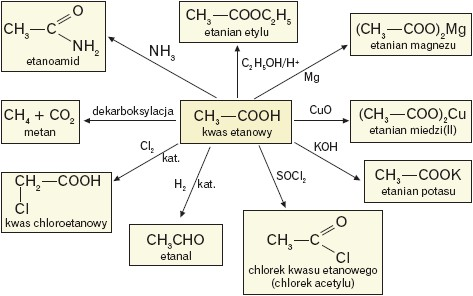
O właściwościach chemicznych kwasów decyduje również charakter reszty węglowodorowej. Jeżeli grupa ta ma charakter nienasycony, to uzyskamy pozytywny wynik reakcji z manganianem(VII) potasu i bromem w środowisku CCl4. Poniżej przedstawiono schematycznie przebieg reakcji z udziałem kwasu pent-3-enowego.
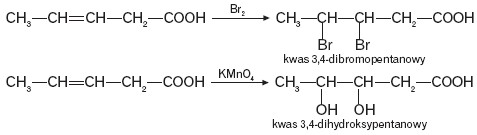
Kwas ten w obecności katalizatora przyłącza wodór, tworząc kwas nasycony.
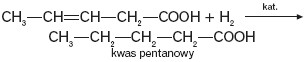
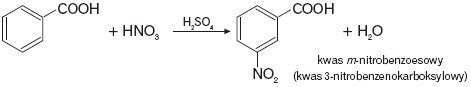
Jeżeli grupa węglowodorowa kwasu zawiera pierścień benzenowy, to kwas ten posiada charakter aromatyczny i ulega np. nitrowaniu. Ponieważ grupa karboksylowa należy do podstawników II rodzaju, jako produkt główny powstaje izomer meta: