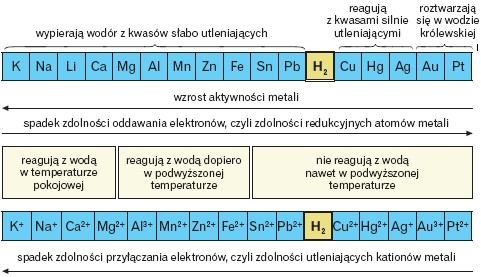
Substancje przewodzące prąd elektryczny to przewodniki. Można je podzielić na:
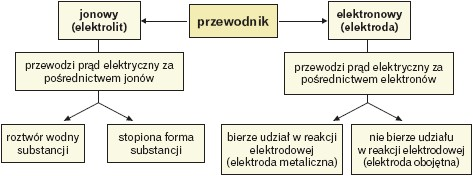
Układ złożony z bezpośrednio stykających się przewodników jonowego i elektronowego to półogniwo. Na granicy metal–roztwór jonów tego metalu tworzy się podwójna warstwa elektryczna, dzięki temu elektroda uzyskuje pewien potencjał elektryczny (tzw. potencjał elektrody), który zależy od rodzaju metalu, rodzaju elektrolitu i stężeń jonów w roztworze.
Ilościowo potencjał takiej elektrody tzw. pierwszego rodzaju określa wzór Nernsta:

Potencjał standardowy elektrody E0Me/Mez+ to potencjał elektrody, zbudowanej z metalu zanurzonego w roztworze, w którym stężenie jonów potencjałotwórczych wynosi 1 mol/dm3 i wszystkie gazy są pod ciśnieniem 1000 hPa, w temperaturze250C (298 K), mierzony w stosunku do standardowej elektrody wodorowej.
Podany wyżej wzór Nernsta jest prawdziwy dla roztworów rozcieńczonych; natomiast dla roztworów stężonych obowiązuje zależność:

Wzór Nernsta można zapisać w formie najbardziej ogólnej:

Poniższy graf i tabelka przedstawiają charakterystykę półogniw:
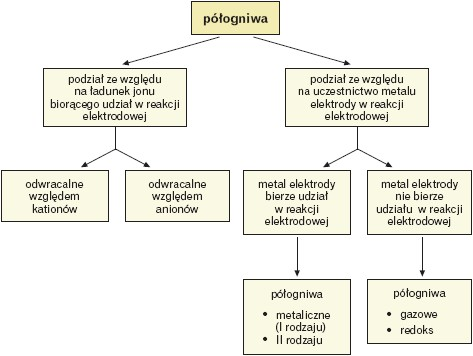


Zestawienie standardowych potencjałów elektrod metalicznych, uporządkowanych według rosnących wartości, tworzy tzw. szereg napięciowy metali:
- ujemna wartość potencjału w szeregu wskazuje, że metal ma większą zdolność do utraty elektronów niż wodór (większa zdolność metalu do utleniania się) – metal jest silniejszym reduktorem,
- najbardziej aktywne metale znajdują się na początku szeregu napięciowego, najmniej aktywne są na końcu (metale szlachetne),
- metal bardziej aktywny wypiera metal mniej aktywny z roztworu jego soli,
- ze wzrostem wartości potencjału rosną właściwości utleniające jonów metali,
- metale o ujemnym potencjale wypierają wodór z kwasów słabo utleniających.