 | ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| Ogólne informacje | ||||||||||||||||||||||||||||||||||||||||||
| Wzór sumaryczny |
C4H4O4 | |||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Inne wzory |
C | |||||||||||||||||||||||||||||||||||||||||
| Masa molowa |
116,07 g/mol | |||||||||||||||||||||||||||||||||||||||||
| Wygląd |
białe lub prawie białe kryształy[1] | |||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | ||||||||||||||||||||||||||||||||||||||||||
| Numer CAS | ||||||||||||||||||||||||||||||||||||||||||
| PubChem | ||||||||||||||||||||||||||||||||||||||||||
| DrugBank | ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | ||||||||||||||||||||||||||||||||||||||||||
| Podobne związki | ||||||||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | ||||||||||||||||||||||||||||||||||||||||||
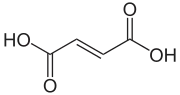
Kwas fumarowy (kwas trans-butenodiowy) – organiczny związek chemiczny z grupy nienasyconych alifatycznych kwasów dikarboksylowych. Występuje w mchach i grzybach. Jest produktem ubocznym metabolizmu węglowodanów. Jego forma zjonizowana (fumaran) występuje jako produkt pośredni w cyklu kwasu cytrynowego (cyklu Krebsa).
Historia
Otrzymany został w 1817 roku niezależnie przez dwóch naukowców – Braconneta i Vauquelina w wyniku pirolizy kwasu jabłkowego[3]. Został też wykryty w borowiku Boletus pseudoignarius[4], a wyizolowany w 1833 roku przez Wincklera z dymnicy pospolitej (Fumaria officinalis, od której wziął swoją nazwę)[5].
Budowa
Jest czterowęglowym kwasem zawierającym w skrajnych pozycjach dwie grupy karboksylowe (−COOH) oraz zawierającym wiązanie podwójne węgiel-węgiel w konfiguracji trans. Jego izomerem geometrycznym o konfiguracji cis jest kwas maleinowy (powstający razem z kwasem fumarowym podczas pirolizy kwasu jabłkowego)[3].
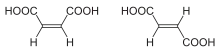
Właściwości
Odbarwia roztwór Br
2 w CCl
4 i wodny roztwór KMnO
4.
W wyniku uwodornienia daje kwas bursztynowy:
- HOOC−CH=CH−COOH + H
2 → HOOC−CH
2−CH
2−COOH
Zastosowanie
Jest stosowany jako lek w łuszczycy. Używany jako dodatek do pasz[6]. Jest stosowany w przemyśle spożywczym jako dodatek do żywności, jego numer to E297 (jako regulator kwasowości, konserwant i przeciwutleniacz).
Otrzymywanie
Na skalę przemysłową kwas fumarowy produkowany jest metodą syntezy chemicznej z bezwodnika kwasu maleinowego, a ten z kolei produkowany jest z butanu.
Rola w organizmach
W organizmach żywych występuje zwykle w formie zjonizowanej, jako fumaran. Najczęściej spełnia rolę organicznego akceptora elektronów, co oznacza, że bierze udział w reakcjach utleniania. Jest jednym z produktów pośrednich w cyklu Krebsa – ulega uwodnieniu (hydratacji) do jabłczanu:
- −
OOC−CH=CH−COO−
+ H
2O → −
OOC−CH
2−CH(OH)−COO−
,
który z kolei przez utlenienie odtwarza szczawiooctan. Jest również produktem ubocznym w cyklu mocznikowym – odłącza się od argininobursztynianu dając argininę, która uwalnia mocznik odtwarzając ornitynę. Zgodnie z powyższym jest zatem ważnym łącznikiem pomiędzy oboma cyklami.
Przypisy
- 1 2 3 4 Farmakopea Polska X, Polskie Towarzystwo Farmaceutyczne, Warszawa: Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, 2014, s. 4276, ISBN 978-83-63724-47-4.
- 1 2 David R. Lide (red.), CRC Handbook of Chemistry and Physics, wyd. 90, Boca Raton: CRC Press, 2009, s. 3-264, ISBN 978-1-4200-9084-0 (ang.).
- 1 2 Goldberg, Israel, Rokem, J Stefan, Pines, Ophry. Organic acids: old metabolites, new themes. „Journal of Chemical Technology & Biotechnology”. 81 (10), s. 1601–1611, 2006. DOI: 10.1002/jctb.1590.
- ↑ Hermann Rudy, Fruchtsäuren. Verlag Hüthig, Heidelberg 1967.
- ↑ Henryk Różański, Fumaria officinalis L. – dymnica lekarska w fitoterapii, [w:] Medycyna dawna i współczesna [online] [dostęp 2015-02-15].
- ↑ Kwas fumarowy – charakterystyka [online], zak.opcom.pl [zarchiwizowane z adresu 2015-02-15]..
![]() Przeczytaj ostrzeżenie dotyczące informacji medycznych i pokrewnych zamieszczonych w Wikipedii.
Przeczytaj ostrzeżenie dotyczące informacji medycznych i pokrewnych zamieszczonych w Wikipedii.
