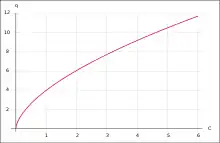
Izoterma Freundlicha – rodzaj empirycznej izotermy adsorpcji, która opisuje adsorpcję na powierzchniach heterogenicznych (energetycznie niejednorodnych) oraz na adsorbentach mikroporowatych.
Różne formy równania Herberta Freundlicha dla adsorpcji z fazy gazowej[1][2][3][4]:
gdzie:
- – adsorpcja rzeczywista,
- – wielkość adsorpcji odpowiadająca zapełnieniu warstwy adsorpcyjnej lub zapełnieniu mikroporów,
- – stała,
- – stała równowagi adsorpcji,
- – ciśnienie adsorbatu,
- – tzw. ciśnienie względne ( – ciśnienie pary nasyconej),
- – empirycznie określone tzw. parametry heterogeniczności ( – im wartość jest mniejsza, tym większa jest niejednorodność energetyczna układu adsorpcyjnego).
Równanie to stosuje się szczególnie do adsorpcji na mikroporowatych węglach aktywnych z rozcieńczonych roztworów wodnych związków organicznych – w powyższych równaniach należy zastąpić ciśnienie stężeniem[1][2][3][4]:
W różnych układach eksperymentalnych obserwowana jest ograniczona zgodność danych adsorpcji z równaniem izotermy Freundlicha (przybliżenie fragmentu krzywej odcinkiem prostej). Niektóre izotermy teoretyczne również redukują się do izotermy Freundlicha (np. izoterma GF dla niskich stężeń). W ramach teorii adsorpcji zlokalizowanej na niejednorodnych energetycznie ciałach stałych izotermie Freundlicha odpowiada eksponencjalnie malejąca funkcja rozkładu energii, jednak w przeciwieństwie do równań opartych na monowarstwowym równaniu Langmuira, izoterma Freundlicha nie zawiera ograniczenia wielkości adsorpcji monowarstwą.
To empiryczne równanie znalazło również pewne uzasadnienie teoretyczne w ramach teorii potencjałowej Euckena i Polanyi’ego oraz teorii objętościowego zapełniania mikroporów (TOZM) Dubinina i Raduszkiewicza (zob. izoterma DR). Może być również uważane za jedno z rozwiązań całkowego równania Stoeckliego. W ramach tych teorii równanie Freundlicha opisuje adsorpcję w mikroporach o określonej strukturze i powinno być przedstawione jako:
- dla
gdzie:
- – pojemność mikroporów (pojemność adsorpcyjna – nie mylić z objętością),
- – parametr strukturalny,
- – ciśnienie przy którym mikropory zostaną całkowicie zapełnione (z reguły niższa niż ciśnienie pary nasyconej),
- – stała gazowa,
- – temperatura.
W układzie logarytmicznym (log(a) od log(c)) dane adsorpcji zgodne z równaniem Freundlicha układają się wzdłuż linii prostej, co pozwala na bardzo łatwe wyznaczanie parametrów równania i opis układów doświadczalnych z pomocą wyznaczonych parametrów[1][2][3][4].
Przypisy
- 1 2 3 17 Zjawiska powierzchniowe. Adsorpcja. W: Stanisław Bursa: Chemia fizyczna. Wyd. 2. Warszawa: PWN, 1979, s. 538–550. ISBN 83-01-00152-6.
- 1 2 3 5. Tarcie graniczne; 5.1. Adsorpcja i chemisorpcja. [w:] Biuletyn PTT, ISSN 1732-422X [on-line]. Polskie Towarzystwo Tribologiczne (PTT). [dostęp 2014-04-10]. [zarchiwizowane z tego adresu (2014-01-28)]. (pol.).
- 1 2 3 Adsorption Isotherm. [w:] Amrita University’s VALUE project [on-line]. amrita.vlab.co.in. [dostęp 2014-04-10]. (ang.).
- 1 2 3 Freundlich Adsorption Isotherm. [w:] Xamplified. Free Online Education Resource > Surface Chemistry [on-line]. www.chemistrylearning.com. [dostęp 2014-04-10]. (ang.).