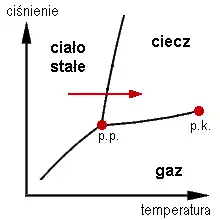

Topnienie – przemiana fazowa polegająca na przejściu substancji ze stanu stałego w stan ciekły[1].
Zjawisko topnienia ściśle wiąże się ze zjawiskiem krzepnięcia. Oznaczana eksperymentalnie temperatura topnienia nie zawsze jednak odpowiada ściśle temperaturze krzepnięcia. Wynika to m.in. z wpływu zanieczyszczeń, szybkości schładzania lub ogrzewania, tworzeniem zarodków krystalizacji oraz ze zjawisk powierzchniowych i międzyfazowych.
Dla każdego idealnie czystego pierwiastka i większości związków chemicznych, przy określonym ciśnieniu można wyznaczyć jedną, ściśle określoną temperaturę topnienia, która zarazem jest też jej temperaturą krzepnięcia. Pomiary takie wykonuje się na bardzo małych próbkach i przy jak najwolniejszym tempie zmiany temperatury. Niektóre związki chemiczne nie topią się w ogóle, gdyż rozkładają się przed osiągnięciem temperatury topnienia.
W przypadku mieszanin związków chemicznych i związków o bardzo wysokich masach cząsteczkowych (polimery, biopolimery), wyznaczanie jednej temperatury topnienia jest niewykonalne, gdyż proces ten jest dla takich substancji bardzo złożony. W przypadku polimerów, kompozytów i stopów metali bardzo często, zamiast mówić o temperaturze topnienia, mówi się raczej o zakresie temperatur mięknięcia.
Z punktu widzenia termodynamiki topnienie jest przemianą fazową I rodzaju, co oznacza w praktyce, że nie może zachodzić bez wymiany ciepła. Procesy topnienia prowadzone pod stałym ciśnieniem mają zawsze charakter endotermiczny, co oznacza, że do ich zajścia konieczne jest dostarczenie z zewnątrz określonej porcji energii termicznej. Ilość ciepła potrzebnego do stopienia danej substancji w temperaturze topnienia jest proporcjonalna do masy tej substancji. Współczynnik proporcjonalności, tzw. ciepło topnienia, jest stały dla danej substancji.
Przypisy
- ↑ topnienie, [w:] Encyklopedia PWN [dostęp 2023-09-14].