| ||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||
| Ogólne informacje | ||||||||||||||||||||||||||||||||||||||||||||||
| Wzór sumaryczny | ||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Inne wzory |
(C | |||||||||||||||||||||||||||||||||||||||||||||
| Masa molowa |
123,11 g/mol | |||||||||||||||||||||||||||||||||||||||||||||
| Wygląd |
bezbarwne kryształy[3] | |||||||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | ||||||||||||||||||||||||||||||||||||||||||||||
| Numer CAS | ||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | ||||||||||||||||||||||||||||||||||||||||||||||
| DrugBank | ||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | ||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||
Witamina B3 (witamina PP) – wspólna nazwa na określenie dwóch związków: kwasu nikotynowego (niacyny, czyli kwasu 3-pirydynokarboksylowego, pochodnej pirydyny) i jego amidu (nikotynamidu), które dla człowieka są witaminą.
- Witamina B3
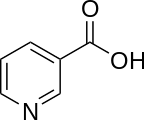 Niacyna
Niacyna
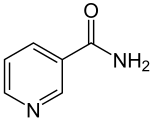 Nikotynamid
Nikotynamid
Niacyna jest znana również jako czynnik przeciwpelagryczny, stąd niekiedy nazywa się ją również witaminą PP. Może być ona, w przeciwieństwie do innych witamin z grupy B, produkowana w organizmie z podstawowego aminokwasu, tryptofanu. Są to jednak niewielkie ilości i jej najważniejszym źródłem powinno być pożywienie. Należy również pamiętać, że tryptofan należy do aminokwasów egzogennych, czyli takich, które nie mogą być syntetyzowane w organizmie, lecz muszą zostać dostarczone w pożywieniu.
Rola w organizmie
Współdziała w syntezie i rozkładzie węglowodanów, kwasów tłuszczowych i aminokwasów, w przemianach metabolicznych mających na celu uwalnianie energii, uczestniczy w tworzeniu krwinek czerwonych, hamuje toksyczne działanie związków chemicznych i leków, reguluje poziom cholesterolu we krwi, rozszerza naczynia krwionośne, oddziałuje korzystnie na system nerwowy i stan psychiczny, poprawia ukrwienie skóry i kondycję włosów.
Zapotrzebowanie dietetyczne
Zalecane dzienne zapotrzebowanie niacyny to 2–12 mg/dzień dla dzieci, 14 mg/dzień dla kobiet, 16 mg/dzień dla mężczyzn oraz 17–18 mg/dzień dla kobiet w ciąży czy też karmiących. Górnym limitem dla dorosłych kobiet i mężczyzn jest 35 mg/dzień. Wartości te oparto na występowaniu mrowienia / zaczerwienienia skóry (flushing) jako krytycznym działaniu ubocznym[7][8].
Poziom niacyny jest zwykle badany w moczu[9], gdyż testy te są uznawane za dokładniejsze niż testy krwi[10].
Przyczyny niedoboru
Na szerszą skalę, niedobór niacyny czasami występuje w rozwijających się krajach, gdzie głównymi czynnikami powodującymi niedobór są niedożywienie / dieta zawierająca małą ilość niacyny/tryptofanu oraz alkoholizm[11]. Zdarza się także w rejonach, gdzie podstawowym pożywieniem jest kukurydza przygotowywana bez procesu nixtamalizacji. Regiony, które tradycyjnie poddają kukurydzę nixtamalizacji, nie mają przypadków niedoboru niacyny.
Do przyczyn niedoboru należą także:
- długotrwałe stosowanie leków przeciwgruźliczych[7] – izoniazydów – które są analogami strukturalnymi niacyny
- choroba Hartnupów – zaburzenie wchłaniania jelitowego i nerkowego tryptofanu
- upośledzone wchłanianie z przewodu pokarmowego
- zwiększone zapotrzebowanie na witaminę spowodowane zwiększeniem ilości procesów energetycznych (na przykład wskutek spożywania dużych ilości cukru)
- nadmierne zużycie tryptofanu do produkcji serotoniny, co ma miejsce w wypadku nowotworu zwanego rakowiakiem[12].
Skutki niedoboru
Małe niedobory niacyny mogą powodować zwolnienie metabolizmu, przez co zmniejszenie tolerancji na zimno.
Duże niedobory niacyny powodują chorobę pelagrę. Charakterystyczne objawy to tzw. „zespół 4d” (dermatitis – zapalenie skóry, diarrhoea – biegunka, dementia – otępienie, death – śmierć). Ponadto mogą występować objawy jak: hiperpigmentacja, zgrubienie skóry, zapalenie jamy ustnej, zapalenie języka, zespół krowiego języka, zaburzenia układu pokarmowego, oraz jeżeli choroba jest nie leczona – śmierć[13]. Mogą też występować następujące objawy psychiatryczne: poirytowanie, słaba koncentracja, amnezja, majaczenie, lęki, zmęczenie, apatia, nadmierna aktywność oraz depresja[13]. Badania wykazały, iż u pacjentów chorych na alkoholową pelagrę niedobór niacyny może być czynnikiem wpływającym na szybkość postępowania objawów.
Przy chorobie Hartnupów dodatkowe objawy to czerwona, łuskowata wysypka oraz zwiększona wrażliwość skóry na światło słoneczne.
Skutki nadmiaru
Farmakologiczne dozy niacyny (1,5–6 g dziennie) mają dermatologiczne efekty uboczne, np. zaczerwienienie, swędzenie, suchość skóry, wysypka – włączając wyprysk oraz acanthosis nigricans. Notowane są również problemy układu pokarmowego, jak niestrawność, nudności oraz ostra niewydolność wątroby. Może także wystąpić hiperglikemia oraz zaburzenia rytmu serca[14].
Zaczerwienienie skóry zazwyczaj trwa około 15 do 30 minut, czasami występuje razem ze swędzeniem – często bolesnym, głównie w miejscach zakrytych odzieżą. Prostaglandyny są mediatorami tych objawów, dlatego też użycie 300 mg aspiryny pół godziny przed braniem niacyny powoduje zmniejszenie tych objawów. Alternatywnie, jedna tabletka dziennie ibuprofenu może złagodzić te objawy. Zaleca się branie niacyny przy posiłkach. Zazwyczaj po kilku tygodniach brania niacyny u większości osób objawy te przestają występować[15]. Niacyna o spowolnionym uwalnianiu także ma słabsze efekty uboczne[16][17]. Według jednych z ostatnich badań, występowanie zaczerwienienia oraz swędzenia było dużo mniejsze przy użyciu niacyny o spowolnionym uwalnianiu[18]. Jednakże dawki ponad 2 g na dzień mogą powodować uszkodzenie wątroby, szczególnie przy użyciu niacyny o spowolnionym działaniu[14]. Zazwyczaj uważa się, że zaczerwienienie ma związek z histaminą, jednakże wykazano, iż histamina nie ma związku z tymi objawami[19]. Prostaglandyny są podstawowym, a serotonina drugorzędnym powodem tych objawów[19].
W badaniach laboratoryjnych wykazano, iż niacyna w dawkach używanych do obniżania cholesterolu może powodować wady wrodzone u testowanych zwierząt. Sugeruje to, że niacyna może mieć zły wpływ na rozwój płodu u ciężarnych kobiet[14].
Efektem ubocznym stosowania dużych dawek niacyny może być hiperurykemia, a przez to pogarszająca się dna moczanowa[20].
Pomimo tego, iż niacyna w większych dawkach zwiększa zawartość glukozy w osoczu, przez co pogarszając cukrzycę[14], ostatnie badania wykazały, że wpływ niacyny na poziom cukru w osoczu nie był większy niż 5–10%[21]. Pacjenci chorzy na cukrzycę, którzy brali lekarstwa na cukrzycę, a także niacynę, nie mieli problemów z brakiem kontroli poziomu cukru. Dlatego też niacyna jest dalej zalecana dla chorych na cukrzycę jako jeden z leków regulujących cholesterol.
W bardzo wysokich dawkach, niacyna może mieć skutki śmiertelne[22]. Bardzo wysokie dawki niacyny mogą powodować zmiany w plamce żółtej, pogrubianie plamki żółtej oraz siatkówki, co prowadzi do pogorszenia i w konsekwencji utraty zdolności widzenia. Jednakże te zmiany są odwracalne po odstawieniu niacyny[23].
Wpływ na regulację cholesterolu
Niacyna blokuje rozpad tłuszczów w tkance tłuszczowej. Tłuszcze te są potrzebne do wytwarzania lipoproteiny bardzo małej gęstości (VLDL) w wątrobie, która to lipoproteina jest prekursorem lipoproteiny niskiej gęstości (LDL) – złego cholesterolu. Ponieważ niacyna blokuje rozpad tłuszczów, powoduje to zmniejszenie poziomu wolnych kwasów tłuszczowych we krwi oraz, w konsekwencji, zmniejszenie wydzielania przez wątrobę VLDL oraz cholesterolu[24].
Poprzez zmniejszanie poziomu VLDL niacyna także powoduje podwyższenie poziomu lipoproteiny wysokiej gęstości (HDL) – „dobrego” cholesterolu we krwi, dlatego też jest czasami przepisywana dla osób z niskim poziomem HDL, które są także w grupie wysokiego ryzyka zawału serca[25][26].
W 1981 r. zaobserwowano, że codzienne przyjmowanie niacyny w dawce 3 × 1 g przez 5 tygodni doprowadziło do spadku poziomu cholesterolu o 22%[27].
Wyniki badań ARBITER 6-HALTS przedstawione przez American Heart Association w 2009 wskazują[28], że niacyna podawana razem ze statynami (dawka 2000 mg/dobę niacyny o spowolnionym uwalnianiu) jest bardziej efektywna od ezetymib w zmniejszaniu grubości ścian tętnicy szyjnej – wskaźnika zaawansowania miażdżycy[29].
Metaanaliza 11 kontrolowanych badań klinicznych przeprowadzona w 2009 roku wykazała, iż niacyna, użyta jako jedyny lek lub też w kombinacji z innymi lekami, znacznie zmniejszyła ilość głównych incydentow chorób wieńcowych (zawałów, udarów mózgu) oraz rozwój miażdżycy[30].
Badania kliniczne z roku 2011 przeprowadzone przez National Heart, Lung, and Blood Institute (NHLBI) zostały przedwcześnie zatrzymane, ponieważ pacjenci wykazywali brak zmniejszenia incydentów chorób wieńcowych, przy czym zwiększyło się ryzyko udarów[31]. Pacjenci będący w grupie testowej mieli już wcześniej dobrze kontrolowany poziom LDL przez statyny. Celem tych badań była ewaluacja podwyższenia poziomu HDL przez niacynę o spowolnionym uwalnianiu (2000 mg/dzień), na incydenty chorób wieńcowych. W badaniach tych niacyna nie miała pozytywnych efektów, natomiast podwyższała ryzyko udarów[32]. Efekty niacyny u pacjentów, u których poziom LDL nie jest kontrolowany (jak w większości poprzednich badań nad niacyną) są dalej badane, jednak badania te wykazały, że niacyna nie daje pozytywnych efektów poprzez podwyższanie poziomu HDL u pacjentów, którzy kontrolują poziom LDL statynami[33].
Heksanikotynian inozytolu
Heksanikotynian inozytolu (HNI) jest często sprzedawany jako suplement diety zawierający niacynę. Jest to inozytol, który został poddany estryfikacji z niacyną na wszystkich sześciu alkoholowych grupach inozytolu. HNI jest zazwyczaj sprzedawany jako niacyna nie powodująca zaczerwienienia/mrowienia (flushing) w dawkach 250, 500 oraz 1000 mg. Jednak reklamowanie oraz sprzedawanie HNI jako niacyny błędnie sugeruje, że HNI jest aktywną formą niacyny. Badania nad właściwościami regulacji lipidów przez HNI są w najlepszym przypadku kontrowersyjne.
Badania kliniczne były przeprowadzane we wczesnych latach 60. (Dorner, Welsh) oraz w latach 70. (Ziliotto, Kruse, Agusti), dlatego też jest je trudno ocenić z perspektywy dzisiejszych standardów[34]. Niektóre badania stwierdzały pozytywne działanie HNI na redukcję kwasów tluszczowch[35], jednakże inne badania przeprowadzane w tym samym czasie nie potwierdzały tych wyników[36].
Najnowsze badania tłumaczą brak wpływu preparatów zawierających HNI na redukcję kwasów tłuszczowych faktem, iż HNI nie zawiera biologicznie przyswajalnej niacyny. Także najnowsze badania porównujące wyniki grupy biorącej przez trzy miesiące dawkę 1500 mg/dzień, do grupy kontrolnej (biorącej placebo) wykazały brak poprawy w poziomach cholesterolu, LDL, HDL oraz trójglicerydów[37].
Z wyżej wymienionych powodów, obecnie nie ma wystarczających dowodów aby polecać IHN do leczenia dyslipidemii aterogennej. Ponadto organizacje American Heart Association oraz National Cholesterol Education Program uważają, że tylko przepisywana niacyna może być używana do leczenia dyslipidemii aterogennej i tylko pod kontrolą lekarską. Podawanym powodem jest fakt, że dawki niacyny o wartości 1500–3000 mg/dzień mogą potencjalnie mieć bardzo niebezpieczne efekty uboczne. Dlatego też powinno się przeprowadzać testy funkcji wątroby (enzymów), przy braniu terapeutycznych dawek niacyny, włączając fosfatazę alkaliczną (ALP), aminotransferazę asparaginianową (AST) oraz aminotransferazę alaninową (ALT).
Biosynteza oraz chemiczna synteza

Wątroba może syntetyzować niacynę z tryptofanu. Synteza ta zależy od enzymów, które wymagają witaminy B6, ryboflawiny, a także enzymów zawierających żelazo. Średnio 1 mg niacyny może być zsyntetyzowany z 60 mg spożytego tryptofanu[7].
Niacyna jest chemicznie syntetyzowana używając 3-metylopirydyny jako prekursora; utleniając 3-metylopirydynę w obecności nadmanganianu potasu (KMnO4)[38].

Niacynę można otrzymać także z chinoliny, utleniając ją w obecności nadmanganianu potasu, gdzie pośrednim produktem jest kwas chinolinowy[39]

Wpływ na receptory
Poza wpływem na NAD oraz NADP, niacyna może mieć dodatkowo wpływ na aktywację receptorów. Receptor reagujący z niacyną jest receptorem GPCR nazwany HM74A[40]. Jest to wiązane do Gi alpha subunit[41].
Źródła witaminy
Występuje powszechnie w produktach roślinnych i zwierzęcych, np. w mięsie, orzechach i ziarnach zbóż. Znaczne ilości niacyny występują w palonych ziarnach kawy, przy czym zawartość ta wyraźnie zwiększa się (nawet trzykrotnie) wraz z intensywnością upalenia[42]. W przypadku niedoboru niacyna może być podawana domięśniowo i doustnie.
Stosunkowo duża jest zawartość niacyny w kukurydzy, jednak jest ona w formie nieprzyswajalnej przez człowieka[43]. Brak objawów pelagry wśród mieszkańców Meksyku, żywiących się głównie kukurydzą, wynika z tradycyjnego sposobu przygotowywania tortilli, który zaczyna się od nixtamalizacji, czyli wymoczenia ziaren kukurydzy w wodzie wapiennej, co powoduje uwolnienie związanej niacyny. Z kolei brak pelagry u rdzennych Amerykanów wynika ze spożywania przez nich niedojrzałej kukurydzy, w której niacyna jest biodostępna[7]. Większość niacyny w kukurydzy (około 60%) znajduje się w zewnętrznej warstwie ziarna, która to warstwa zazwyczaj zostaje usuwana w procesie produkcji mąki[44].
Historia
Niacyna została pierwszy raz opisana przez Hugo Weidela w 1873 roku, w jego opracowaniach z badań nad nikotyną[45]. Została ona wyodrębniona z wątroby przez Konrada Elvehjema, który zidentyfikował jej aktywny składnik, a następnie nazywał go „czynnikiem zapobiegającym pelagrze” oraz „czynnikiem zapobiegającym zespołowi krowiego języka”[46].
Kiedy biologiczne znaczenie kwasu nikotynowego zostało odkryte, postanowiono zmienić nazwę kwasu nikotynowego. Zmiana ta, miała na celu podkreślenie, że nie ma związku pomiędzy bogatą w niacynę żywnością a nikotyną, a także pomiędzy nikotyną a witaminami. W rezultacie tego angielska nazwa niacyny – niacin – została złożona z nicotinic acid + vitamin.
Niacyna jest nazywana witaminą B3, ponieważ była odkryta jako trzecia witamina z grupy witamin B. Niacyna jest też nazywana witaminą PP od pierwotnej anglojęzycznej nazwy „Pellagra-Preventing factor”.
Przypisy
- 1 2 Henri A. Favre, Warren H. Powell, Nomenklatura związków organicznych. Rekomendacje IUPAC i nazwy preferowane 2013, Komisja Terminologii Chemicznej Polskiego Towarzystwa Chemicznego (tłum.), wyd. 1, Narodowy Komitet Międzynarodowej Unii Chemii Czystej i Stosowanej, [2016], s. 706.
- ↑ Farmakopea Polska IX, Polskie Towarzystwo Farmaceutyczne, Warszawa: Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych, 2011, s. 4574, ISBN 978-83-88157-77-6.
- 1 2 Nicotinic acid, [w:] PubChem, United States National Library of Medicine, CID: 938 (ang.).
- 1 2 CRC Handbook of Chemistry and Physics, David R. Lide (red.), wyd. 88, Boca Raton: CRC Press, 2007, s. 3-450, ISBN 978-0-8493-0488-0 (ang.).
- ↑ Witamina B3 (nr N4126) (ang.) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Stanów Zjednoczonych.
- ↑ Witamina B3 (nr 72309) w katalogu produktów Sigma-Aldrich (Merck).
- 1 2 3 4 Niacin [online], Linus Pauling Institute, Oregon State University [dostęp 2022-05-15] (ang.).
- ↑ USDA National Nutrient Database for Standard Reference, Release 22. Niacin (mg) Content of Selected Foods per Common Measure, sorted by nutrient content [online], Departament Rolnictwa USA (ang.).
- ↑ Niacin, [w:] Dietary Reference Intakes Research Synthesis: Workshop Summary [online], National Academies Press, s. 37–38 [dostęp 2017-03-02] (ang.).
- ↑ R.A. Jacob i inni, Biochemical markers for assessment of niacin status in young men: urinary and blood levels of niacin metabolites, „The Journal of Nutrition”, 119 (4), 1989, s. 591–598, DOI: 10.1093/jn/119.4.591, PMID: 2522982 [dostęp 2021-04-06] (ang.).
- ↑ Stergios Pitsavas i inni, Pellagra encephalopathy following B-complex vitamin treatment without niacin, „International Journal of Psychiatry in Medicine”, 34 (1), 2004, s. 91–95, DOI: 10.2190/29XV-1GG1-U17K-RGJH, PMID: 15242145 [dostęp 2021-04-06] (ang.).
- ↑ Girish M. Shah i inni, Biochemical assessment of niacin deficiency among carcinoid cancer patients, „The American Journal of Gastroenterology”, 100 (10), 2005, s. 2307–2314, DOI: 10.1111/j.1572-0241.2005.00268.x, PMID: 16181385 [dostęp 2021-04-06] (ang.).
- 1 2 Ravi Prakash i inni, Rapid resolution of delusional parasitosis in pellagra with niacin augmentation therapy, „General Hospital Psychiatry”, 30 (6), 2008, s. 581–584, DOI: 10.1016/j.genhosppsych.2008.04.011, PMID: 19061687 (ang.).
- 1 2 3 4 Keith Parker i inni, Goodman & Gilman’s the pharmacological basis of therapeutics, New York: McGraw-Hill, 2006, ISBN 0-07-142280-3.
- ↑ Guidelines for Niacin Therapy For the Treatment of Elevated Lipoprotein a (Lpa) [online], Rush University Medical Center, 15 sierpnia 2002 [zarchiwizowane z adresu 2011-07-22], Cytat: facial flushing is a common side effect of niacin therapy that usually subsides after several weeks of consistent niacin use, Aktualizacja 27 lipca 2005.
- ↑ Bertram G. Katzung, Basic and clinical pharmacology, New York: McGraw-Hill Medical Publishing Division, 2006, ISBN 0-07-145153-6.
- ↑ Philip Barter, Options for therapeutic intervention: how effective are the different agents?, „European Heart Journal Supplements”, 8 (suppl_F), 2006, F47–F53, DOI: 10.1093/eurheartj/sul041 (ang.).
- ↑ M. John Chapman i inni, Raising high-density lipoprotein cholesterol with reduction of cardiovascular risk: the role of nicotinic acid–a position paper developed by the European Consensus Panel on HDL-C, „Current Medical Research and Opinion”, 20 (8), 2004, s. 1253–1268, DOI: 10.1185/030079904125004402, PMID: 15324528 [dostęp 2021-04-06] (ang.).
- 1 2 Dean Papaliodis i inni, Niacin-induced „flush” involves release of prostaglandin D2 from mast cells and serotonin from platelets: evidence from human cells in vitro and an animal model, „The Journal of Pharmacology and Experimental Therapeutics”, 327 (3), 2008, s. 665–672, DOI: 10.1124/jpet.108.141333, PMID: 18784348 [dostęp 2021-04-06] (ang.).
- ↑ D.M. Capuzzi i inni, Niacin dosing: relationship to benefits and adverse effects, „Current Atherosclerosis Reports”, 2 (1), 2000, s. 64–71, DOI: 10.1007/s11883-000-0096-y, PMID: 11122726 [dostęp 2021-04-06] (ang.).
- ↑ M.B. Elam i inni, Effect of niacin on lipid and lipoprotein levels and glycemic control in patients with diabetes and peripheral arterial disease: the ADMIT study: A randomized trial. Arterial Disease Multiple Intervention Trial, „Journal of the American Medical Association”, 284 (10), 2000, s. 1263–1270, DOI: 10.1001/jama.284.10.1263, PMID: 10979113 [dostęp 2022-05-15] (ang.).
- ↑ Manoj K. Mittal i inni, Toxicity from the use of niacin to beat urine drug screening, „Annals of Emergency Medicine”, 50 (5), 2007, s. 587–590, DOI: 10.1016/j.annemergmed.2007.01.014, PMID: 17418450 [dostęp 2021-04-06] (ang.).
- ↑ J. Donald M. Gass, Nicotinic acid maculopathy. 1973, „Retina”, 23 (6 Suppl), 2003, s. 500–510, PMID: 15035390 [dostęp 2021-04-06] (ang.).
- ↑ Omudhome Ogbru, niacin (Niacor, Niaspan) [online], MedicineNet [dostęp 2022-05-15].
- ↑ Mark E. McGovern, Taking aim at HDL-C. Raising levels to reduce cardiovascular risk, „Postgraduate Medicine”, 117 (4), 2005, 29–30, 33–35, 39 passim, DOI: 10.3810/pgm.2005.04.1610, PMID: 15842130 [dostęp 2021-04-06] (ang.).
- ↑ P.L. Canner i inni, Fifteen year mortality in Coronary Drug Project patients: long-term benefit with niacin, „Journal of the American College of Cardiology”, 8 (6), 1986, s. 1245–1255, DOI: 10.1016/s0735-1097(86)80293-5, PMID: 3782631 [dostęp 2021-04-06] (ang.).
- ↑ S.M. Grundy i inni, Influence of nicotinic acid on metabolism of cholesterol and triglycerides in man, „Journal of Lipid Research”, 22 (1), 1981, s. 24–36, PMID: 7217784 [dostęp 2022-05-15] (ang.).
- ↑ Allen J. Taylor i inni, Extended-release niacin or ezetimibe and carotid intima-media thickness, „The New England Journal of Medicine”, 361 (22), 2009, s. 2113–2122, DOI: 10.1056/NEJMoa0907569, PMID: 19915217 [dostęp 2021-04-06] (ang.).
- ↑ Natasha Singer, Study Raises Questions About Cholesterol Drug’s Benefit [online], The New York Times, 15 listopada 2009 [zarchiwizowane z adresu 2011-12-25].
- ↑ Eric Bruckert, Julien Labreuche, Pierre Amarenco, Meta-analysis of the effect of nicotinic acid alone or in combination on cardiovascular events and atherosclerosis, „Atherosclerosis”, 210 (2), 2010, s. 353–361, DOI: 10.1016/j.atherosclerosis.2009.12.023, PMID: 20079494 [dostęp 2021-04-06] (ang.).
- ↑ NIH stops clinical trial on combination cholesterol treatment [online], NIH, 26 maja 2011 [dostęp 2022-05-15].
- ↑ Scott Hensley, Boosting Good Cholesterol With Niacin Did Not Cut Heart Risks [online], 26 maja 2011 [dostęp 2011-08-30].
- ↑ Stefan Schandelmaier i inni, Niacin for primary and secondary prevention of cardiovascular events, „The Cochrane Database of Systematic Reviews”, 6, 2017, art. nr CD009744, DOI: 10.1002/14651858.CD009744.pub2, PMID: 28616955, PMCID: PMC6481694 [dostęp 2021-04-06] (ang.).
- ↑ R. Taheri, No-Flush Niacin for the Treatment of Hyperlipidemia [online], Medscape, 15 stycznia 2003 [dostęp 2011-07-22].
- ↑ W. Kruse i inni, Nocturnal inhibition of lipolysis in man by nicotinic acid and derivatives, „European Journal of Clinical Pharmacology”, 16 (1), 1979, s. 11–15, DOI: 10.1007/BF00644960, PMID: 499296 [dostęp 2021-04-06] (ang.).
- ↑ C. Daniel Meyers i inni, Varying cost and free nicotinic acid content in over-the-counter niacin preparations for dyslipidemia, „Annals of Internal Medicine”, 139 (12), 2003, s. 996–1002, DOI: 10.7326/0003-4819-139-12-200312160-00009, PMID: 14678919 [dostęp 2021-04-06] (ang.).
- ↑ Alexandre M. Benjó i inni, Accumulation of chylomicron remnants and impaired vascular reactivity occur in subjects with isolated low HDL cholesterol: effects of niacin treatment, „Atherosclerosis”, 187 (1), 2006, s. 116–122, DOI: 10.1016/j.atherosclerosis.2005.08.025, PMID: 16458316 [dostęp 2021-04-06] (ang.).
- ↑ Harold Hart i inni, Organische Chemie, wyd. 3, Weinheim: Wiley-VCH, 2007, s. 494, ISBN 978-3-527-31801-8 (niem.).
- ↑ Andrew Streitwieser, Clayton H. Heathcock, Edward M. Kosower, Organische Chemie, wyd. 2, Weinheim: Wiley-VCH, 1994, s. 1227, ISBN 3-527-29005-2 (niem.).
- ↑ Youyan Zhang i inni, Niacin mediates lipolysis in adipose tissue through its G-protein coupled receptor HM74A, „Biochemical and Biophysical Research Communications”, 334 (2), 2005, s. 729–732, DOI: 10.1016/j.bbrc.2005.06.141, PMID: 16018973 [dostęp 2021-04-06] (ang.).
- ↑ Christian Zellner i inni, Variations in human HM74 (GPR109B) and HM74A (GPR109A) niacin receptors, „Human Mutation”, 25 (1), 2005, s. 18–21, DOI: 10.1002/humu.20121, PMID: 15580557 [dostęp 2021-04-06] (ang.).
- ↑ I. V.: Nieznane dotychczas korzyści z kawy palonej – kawa contra pelagra, [w:] „Wszechświat. Pismo przyrodnicze” Z. 10 (1914), październik 1960, s. 278.
- ↑ J. Laguna, K.J. Carpenter, Raw versus processed corn in niacin-deficient diets, „The Journal of Nutrition”, 45 (1), 1951, s. 21–28, DOI: 10.1093/jn/45.1.21, PMID: 14880960 [dostęp 2021-04-06] (ang.).
- ↑ Diety oparte na kukurydzy: mineraly i witaminy. [dostęp 2011-07-23]. (ang.).
- ↑ H. Weidel, Zur Kenntniss des Nicotins, „Justus Liebig’s Annalen der Chemie und Pharmacie”, 165 (2), 1873, s. 328–349, DOI: 10.1002/jlac.18731650212 [dostęp 2021-04-06] (niem.).
- ↑ C.A. Elvehjem i inni, The isolation and identification of the anti-black tongue factor, „Journal of Biological Chemistry”, 123 (1), 1938, s. 137–149, DOI: 10.1016/S0021-9258(18)74164-1 [dostęp 2021-04-06] (ang.).
![]() Przeczytaj ostrzeżenie dotyczące informacji medycznych i pokrewnych zamieszczonych w Wikipedii.
Przeczytaj ostrzeżenie dotyczące informacji medycznych i pokrewnych zamieszczonych w Wikipedii.
