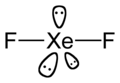| ||||||||||||||||||||||||||||||||||||||||
 Sieć krystaliczna XeF 2 | ||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||
| Ogólne informacje | ||||||||||||||||||||||||||||||||||||||||
| Wzór sumaryczny |
XeF | |||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa |
169,29 g/mol | |||||||||||||||||||||||||||||||||||||||
| Wygląd |
bezbarwne kryształy | |||||||||||||||||||||||||||||||||||||||
| Identyfikacja | ||||||||||||||||||||||||||||||||||||||||
| Numer CAS | ||||||||||||||||||||||||||||||||||||||||
| PubChem | ||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||
| Podobne związki | ||||||||||||||||||||||||||||||||||||||||
| Podobne związki | ||||||||||||||||||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | ||||||||||||||||||||||||||||||||||||||||
Difluorek ksenonu, XeF
2 – nieorganiczny związek chemiczny z grupy fluorków, w którym ksenon występuje na II stopniu utlenienia.
Budowa
Na podstawie analizy widm oscylacyjnych wysokiej rozdzielczości ustalono, że XeF
2 tworzy liniowe cząsteczki o długości wiązań 1,9773 ± 0,0015 Å w fazie gazowej[6], natomiast w wyniku badań wykorzystujących dyfrakcję neutronów oceniono długość wiązania Xe−F w fazie stałej na 2 Å[7]. W strukturze krystalicznej, obok dwóch atomów fluoru związanych chemicznie, ksenon ma w swoim otoczeniu 8 atomów fluoru w odległości obliczonej na 3,64 Å[7] lub 3,42 Å[8]. Każdy atom fluoru ma jednego bliźniaczego sąsiada w odległości 3,02 Å oraz 4 atomy fluoru odległe o 3,08 Å[7]. Upakowanie atomów w stałym XeF
2 jest takie, że ligandy fluorowe sąsiednich cząsteczek unikają strefy równikowej atomu ksenonu ponieważ w cząsteczce XeF
2 trzy niewiążące elektrony efektywnie maskują dodatni ładunek[2]. Występowanie silnych oddziaływań elektrostatycznych pomiędzy cząsteczkami w tak uporządkowanej sieci krystalicznej difluorku ksenonu jest zgodne z jego dość wysoką entalpią sublimacji, która wynosi 55,71 kJ/mol[2][9].
Opublikowane zostały doniesienia, że pod ciśnieniem 50 GPa (ok. 500 tys. atm) XeF
2 ulega przemianie i nabiera właściwości półprzewodzących, a jego niemolekularna już wówczas struktura złożona z dwuwymiarowych warstw zawierających jednostki XeF
4 jest podobna do struktury grafitu. Z przedstawionych rezultatów badań wynika również, że pod wpływem jeszcze wyższego ciśnienia (powyżej 70 GPa) difluorek ksenonu nabiera własności metalicznych, zmieniając swoją strukturę na trójwymiarową, złożoną z elementów XeF
8[10]. Jednakże przedstawione później wyniki prac teoretycznych podważają rezultaty tych prac doświadczalnych – wynika z nich, że tetragonalna struktura przestrzenna I4/mmm upakowania cząsteczek XeF
2 powinna być stabilna aż do ciśnienia 105 GPa, a następnie ulec przemianie do struktury molekularnej odznaczającej się rombową symetrią przestrzenną Pnma, w której długości obu wiązań Xe−F przestają być jednakowe. Dalsza kompresja do 200 GPa będzie według teoretyków skutkowała autodysocjacją do jonowego ciała stałego o przykładowej budowie typu [XeF]+
F−
[11].
Otrzymywanie
Jest to jeden z pierwszych otrzymanych związków chemicznych ksenonu. Jego uzyskanie było efektem wzmożonych prac nad związkami tego gazu szlachetnego po udanej syntezie heksafluoroplatynianu ksenonu[12]. Został on otrzymany latem 1962 roku przez grupę Rudolfa Hoppego z Uniwersytetu w Münster w wyniku reakcji gazowego fluoru z ksenonem pod wpływem wyładowań elektrycznych, a publikacja na temat tego odkrycia ukazała się w listopadzie tego samego roku[13][14]. Praktycznie jednocześnie, w sierpniu 1962 roku, badacze amerykańscy uzyskali niezależnie i opisali inny związek ksenonu i fluoru, tetrafluorek ksenonu, XeF
4. Powstał on w wyniku ogrzewania lub naświetlania promieniowaniem ultrafioletowym mieszaniny ksenonu i fluoru w fazie gazowej. Podczas badań nad XeF
4 zarejestrowano dane spektralne świadczące o powstawaniu trwałego difluorku ksenonu[14][15][16].
XeF
2 można otrzymać bezpośrednio z pierwiastków w fazie gazowej, pod wpływem promieniowania ultrafioletowego[2][17] (również wykorzystując w tym celu światło słoneczne), skoncentrowanego promieniowania γ, elektronów pochodzących z akceleratora van de Graffa, protonów o energii 10 MeV, ciepła[2] oraz wyładowań elektrycznych[2][17]:
- Xe + F
2 → XeF
2↓
Powstający związek wydziela się w postaci stałej, co pozwala na prowadzenie procesu w trybie ciągłym i uzyskiwanie związku w skali kilogramowej. W celu uniknięcia powstawania XeF
4, reakcję prowadzi się przy pewnym nadmiarze ksenonu (jest to istotne z punktu widzenia bezpieczeństwa, gdyż podczas pracy z wykorzystaniem XeF
2 zanieczyszczonego nawet małymi ilościami XeF
4, w wyniku hydrolizy tego ostatniego powstaje wybuchowy XeO
3)[17].
Związek jest także dostępny komercyjnie[17].
Właściwości

Difluorek ksenonu jest ciałem stałym. Tworzy bezbarwne kryształy tetraedryczne o gęstości 4,32 g/cm³[1]. Pod ciśnieniem atmosferycznym sublimuje w temperaturze 114,35 °C[1] (ze względu na łatwość sublimacji praca z tym związkiem wymaga ostrożności)[17]. Temperatura topnienia wynosi ok. 129 °C[3] (w punkcie potrójnym jest to 129,03 °C)[1]. Ma ostry zapach zbliżony do chloru. Jest silnie reaktywny[17]. Ulega rozkładowi pod wpływem światła oraz powolnej hydrolizie w kontakcie z wilgocią[18].
Zastosowanie
XeF
2 jest silnym czynnikiem fluorującym i utleniającym[19][20]. Ze względu na stały stan skupienia jest wygodniejszy i bezpieczniejszy w pracy niż fluor pierwiastkowy; w większości zastosowań można go używać w aparaturze szklanej (niszczonej przez F
2)[17]. Pośród istotnych zastosowań można wymienić:
- Reakcje utleniającego fluorowania:
- Ph
3TeF + XeF
2 → Ph
3TeF
3 + Xe
- Ph
- Reakcje redukcyjnego fluorowania:
- 2CrO
2F
2 + XeF
2 → 2CrOF
3 + Xe + O
2
- 2CrO
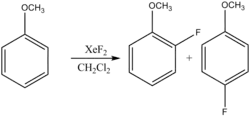
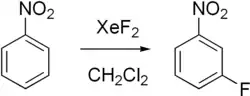
- Reakcje fluorowania związków aromatycznych:
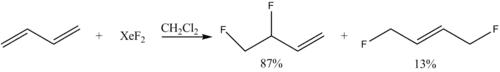
- Reakcje fluorowania alkenów:
- Suche trawienie mikroukładów krzemowych[21], np. do wytwarzania mikroukładów elektromechanicznych[22][23]. Technika została zaprezentowana w 1995 roku[24], a następnie skomercjalizowana[25]. Proces polega na trawieniu krzemu za pomocą XeF
2 w fazie gazowej. Reakcję prowadzi się w temperaturze pokojowej pod obniżonym ciśnieniem[21]:- 2XeF
2 + Si → 2 Xe↑ + SiF
4↑
- 2XeF
Przypisy
- 1 2 3 4 5 CRC Handbook of Chemistry and Physics, David R. Lide (red.), wyd. 88, Boca Raton: CRC Press, 2007, s. 4-98, ISBN 978-0-8493-0488-0 (ang.).
- 1 2 3 4 5 6 7 Melita Tramšek, Boris Žemva. Synthesis, Properties and Chemistry of Xenon(II) Fluoride. „Acta Chimica Slovenica”. 53 (2), s. 105–116, 2006. DOI: 10.1002/chin.200721209.
- 1 2 D.K. Hindermann, W.E. Falconer. Magnetic Shielding of 19
F in XeF
2. „Journal of Chemical Physics”. 50 (3), 1969. DOI: 10.1063/1.1671178. Bibcode: 1969JChPh..50.1203H. - ↑ Difluorek ksenonu (nr 394505) (ang.) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Stanów Zjednoczonych. [dostęp 2016-08-23]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- 1 2 3 Difluorek ksenonu (nr 394505) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Polski. [dostęp 2016-08-23]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ Sandor Reichman. Gas-Phase Structure of XeF
2. „Journal of Chemical Physics”. 51 (6), s. 2355–2359, 1969. DOI: 10.1063/1.1672351. - 1 2 3 Henri A. Levy, P.A. Agron. The Crystal and Molecular Structure of Xenon Difluoride by Neutron Diffraction. „Journal of the American Chemical Society”. 85 (2), s. 241–242, 1963. DOI: 10.1021/ja00885a037.
- ↑ P.A. Agron i inni, Xenon Difluoride and the Nature of the Xenon-Fluorine Bond, „Science”, 3557, 139, 1963, s. 842–844, DOI: 10.1126/science.139.3557.842.
- ↑ Joshua. Jortner, E. Guy. Wilson, Stuart A. Rice. The Heats of Sublimation of XeF
2 and XeF
4 and a Conjecture on Bonding in The Solids. „Journal of the American Chemical Society”. 85 (6), s. 814–815, 1963. DOI: 10.1021/ja00889a034. - ↑ Minseob Kim, Mathew Debessai, Choong-Shik Yoo. Two- and three-dimensional extended solids and metallization of compressed XeF. „Nature Chemistry”. 2 (9), s. 784–788, 2010. DOI: 10.1038/nchem.724.
- ↑ Dominik Kurzydłowski, Patryk Zaleski-Ejgierd, Wojciech Grochala, Roald Hoffmann. Freezing in Resonance Structures for Better Packing: XeF
2 Becomes (XeF+
)(F−
) at Large Compression. „Inorganic Chemistry”. 50 (8), s. 3832–3840, 2011. DOI: 10.1021/ic200371a. - ↑ N. Bartlett. Xenon hexafluoroplatinate(V) Xe+
[PtF
6]−
. „Proceedings of the Chemical Society”. 6, s. 218, 1962. DOI: 10.1039/PS9620000197. - ↑ R. Hoppe, W. Daehne, H. Mattauch, K Roedder. Fluorination of Xenon. „Angewandte Chemie International Edition in English”. 1 (11), s. 599, 1962. DOI: 10.1002/anie.196205992.
- 1 2 R. Hoppe. Valence Compounds of the Inert Gases. „Angewandte Chemie International Edition in English”. 3 (8), s. 538–545, 1964. DOI: 10.1002/anie.196405381.
- ↑ Howard H. Claassen, Henry Selig, John G. Malm. Xenon Tetrafluoride. „Journal of the American Chemical Society”. 84 (18), s. 3593–3593, 1962. DOI: 10.1021/ja00877a042.
- ↑ C.L. Chernick i inni, Fluorine Compounds of Xenon and Radon, „Science”, 3537, 138, 1962, s. 136–138, DOI: 10.1126/science.138.3537.136.
- 1 2 3 4 5 6 7 Marcus A. Tius. Xenon difluoride in synthesis. „Tetrahedron”. 51 (24), s. 6605–6634, 1995. DOI: 10.1016/0040-4020(95)00362-C.
- ↑ James L. Weeks, Max S. Matheson. Xenon Difluoride. „Inorganic Syntheses”. 8. s. 260–264. DOI: 10.1002/9780470132395.ch69.
- ↑ D.F. Halpem: Xenon(II) Fluoride. W: Encyclopedia of Reagents for Organic Synthesis. L. Paquette (red.). New York: John Wiley & Sons, 2004. DOI: 10.1002/047084289X.rx001.
- ↑ S. Taylor, C. Kotoris, G. Hum. Recent Advances in Electrophilic Fluorination. „Tetrahedron”. 55 (43), s. 12431–12477, 1999. DOI: 10.1016/S0040-4020(99)00748-6.
- 1 2 J.D. Brazzle, M.R. Dokmeci, C.H Mastrangelo. Modeling and characterization of sacrificial polysilicon etching using vapor-phase xenon difluoride. „Materiały 17th IEEE International Conference on MEMS”, s. 737–740, 2004. DOI: 10.1109/MEMS.2004.1290690.
- ↑ XERIC™ Silicon Etch. memsstar Limited. [dostęp 2015-08-11]. (ang.).
- ↑ XactiX Xenon Difluoride Etcher. Maryland NanoCenter, University of Maryland. [dostęp 2015-08-11]. (ang.).
- ↑ Floy I. Chang, Richard Yeh, Gisela Lin, Patrick B. Chu i inni. Gas-phase silicon micromachining with xenon difluoride. „SPIE Proceedings”. 2641, s. 117–128, 1995. DOI: 10.1117/12.220933.
- ↑ P. Chu i inni, Controlled Pulse-Etching with Xenon Difluoride, „International Conference on Solid State Sensors and Actuators, TRANSDUCERS '97”, Chicago 1997, s. 665–668, DOI: 10.1109/SENSOR.1997.613739.