| |||||||||||||
| Ogólne informacje | |||||||||||||
| Wzór sumaryczny |
C21H36N7O16P3S | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa |
767,53 g/mol | ||||||||||||
| Identyfikacja | |||||||||||||
| Numer CAS | |||||||||||||
| PubChem | |||||||||||||
| DrugBank | |||||||||||||
| |||||||||||||
| |||||||||||||
Koenzym A (CoA, CoA∼SH) – organiczny związek chemiczny zbudowany z reszt 3′-fosforyloadenozynodifosforanu, pantotenianu i cysteaminy. W organizmach żywych służy jako przenośnik grup acylowych, które wiążą się do niego poprzez grupę tiolową (−SH). Cząsteczkę koenzymu A związaną z resztą acylową nazywa się acylokoenzymem A (acylo-CoA). Najważniejszym z takich połączeń jest acetylokoenzym A (acetylo-CoA).

(1) adenozyno-3′-fosforan, (2) pirofosforan, (3) kwas pantoinowy, (4) β-alanina, (5) cysteamina
przy czym: (1)+(2) 3′-fosforan ADP, (3)+(4) kwas pantotenowy, (3)+(4)+(5) panteteina
Biosynteza
Biosynteza CoA przebiega w taki sam sposób u prokariontów i eukariontów i obejmuje pięć etapów, w których wykorzystywane są 4 cząsteczki ATP[1]:
- fosforylację pantotenianu w pozycji 4'
- przyłączenie cysteiny do grupy karboksylowej
- dekarboksylacja reszty cysteiny
- przyłączenie reszty AMP do grupy fosforanowej
- fosforylacja grupy 3′-hydroksylowej adenozyny.
Acylo-CoA i acetylo-CoA
Acylo-CoA, czyli acylokoenzym A to połączenie koenzymu A z resztą acylową umożliwiające jej transport w organizmie. Przenosi on grupy acylowe o długości wahającej się między 2 a 24 węglami lub nawet dłuższe elementy. Acylo-CoA powstaje w wyniku acylowania grupy tiolowej CoA:
- CoASH + RCOOH → CoAS~COR + H2O
Najważniejszym przykładem takiego połączenia jest acetylokoenzym A (acetyl-CoA), tzw. aktywny octan – produkt acetylowania koenzymu A, uczestniczący w wielu przemianach zachodzących w organizmie, np. w cyklu kwasu cytrynowego.
Acetylo-CoA odgrywa kluczową rolę w metabolizmie. Składa się z grupy acetylowej (−COCH
3) związanej kowalencyjnie z koenzymem A. Jest on na przykład bezpośrednio wykorzystywany przez połączenie z kwasem szczawiooctowym do syntezy kwasu cytrynowego, który rozpoczyna cykl kwasu cytrynowego (kwasów trójkarboksylowych). W postaci aktywnego octanu kwas octowy łączy się także z choliną, tworząc acetylocholinę, lub z sulfonamidami, które przed wydaleniem ulegają acetylacji. Acetylokoenzym A odgrywa również ważną rolę w metabolizmie lipidów – jest prekursorem cholesterolu, a tym samym hormonów steroidowych[2].
Tworzenie acetylo-CoA w mitochondriach
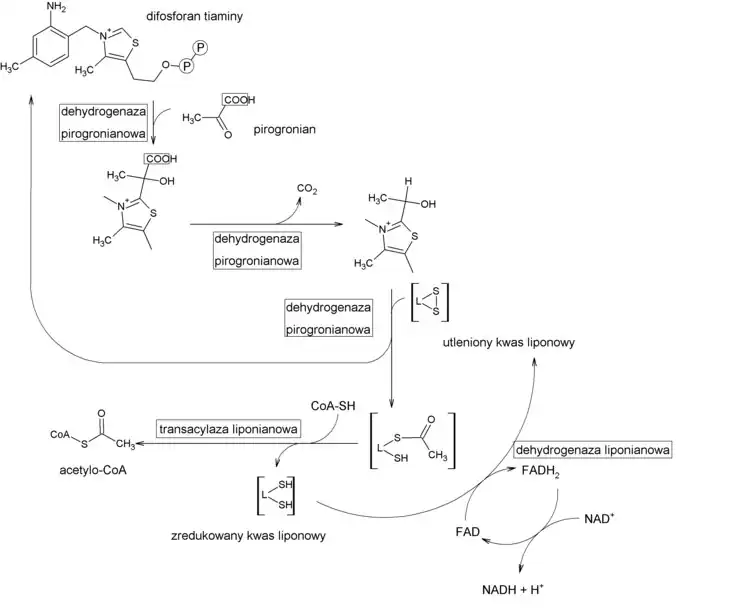
Pirogronian po wejściu do mitochondriów może ulec utlenieniu do CO2 i H2O (w cyklu kwasów trójkarboksylowych), bądź być wykorzystany do syntezy kwasów lub innych związków. Uprzednio jednak musi ulec utleniającej dekarboksylacji, tworząc „aktywny octan” – acetylo-CoA.
Faktyczny mechanizm reakcji jest znacznie bardziej złożony. W katalizującym kompleksie uczestniczą trzy enzymy główne (dehydrogenaza pirogronianowa, transacylaza liponianowa, dehydrogenaza liponianowa), pięć koenzymów (pirofosforan tiaminy, kwas liponowy, NAD+, FAD, CoA) oraz dwa enzymy regulujące (kinaza i fosfataza dehydrogenazy pirogronianowej).
Przebieg procesu zależy od stanu energetycznego komórki. Przy wysokim stężeniu ATP dehydrogenaza pirogronianowa przy udziale odpowiedniej kinazy przechodzi w nieaktywną formę ufosforylowaną, dzięki czemu cały proces ulega zahamowaniu. Przy niskim stężeniu ATP, o wysokim ADP oraz Ca2+ następuje pod wpływem swoistej fosfatazy defosforylacja dehydrogenazy pirogronianowej, z utworzeniem formy aktywnej enzymu.
Proces utleniającej dekarboksylacji α-ketokwasów jest źródłem czterech wiązań wysokoenergetycznych. Trzy tworzone są podczas utleniania poprzez łańcuch oddechowy powstałego NADH. Czwarte, powstałe na poziomie substratu, zmagazynowane jest w postaci ~S-CoA. Przy dekarboksylacji pirogronianu wiązanie to nie jest źródłem ATP, jest jednak wykorzystywane w procesach syntezy. Proces utleniającej dekarboksylacji pirogronianu jest nieodwracalny.
Przypisy
- ↑ Leonardi, Roberta, Zhang, Yong-Mei, Rock, Charles O., Jackowski, Suzanne. Coenzyme A: Back in action. „Progress in Lipid Research”. 44 (2–3), s. 125–153, 2005. DOI: 10.1016/j.plipres.2005.04.001.
- ↑ H. Harper, V. Rodwell: Zarys chemii fizjologicznej. Wyd. II. Warszawa: Państwowy Zakład Wydawnictw Lekarskich, 1983, s. 976. ISBN 83-200-0499-3.
Bibliografia
- R. Murray, P. Mayes, V. Rodwell: Biochemia Harpera. Wyd. III. Warszawa: Wydawnictwo Lekarskie PZWL, 1995, s. 955. ISBN 83-200-1798-X.
- Lubert Stryer: Biochemia. Wyd. IV. Warszawa: Wydawnictwo Naukowe PWN, 2003, s. 1132.
